Divulgación
Curas sin dolor
Publicado
hace 4 añosel

Índice
- 1 Curas sin dolor
Curas sin dolor
Según la Asociación Internacional para el Estudio del Dolor, de las definiciones existentes, una de las más difundidas y aceptadas es: «El dolor es una experiencia sensorial y emocional desagradable, asociada a una lesión tisular real o potencial, o que se describe como ocasionada por dicha lesión». En CMUC realizamos curas en heridas y úlceras que se han complicado e intentamos que sean sin dolor o con la mínima molestia posible.
El dolor es compañero inseparable del ser humano desde el inicio mismo de la vida, la búsqueda de remedios para remitir su intensidad ha estado presente en cada una de las civilizaciones que han poblado nuestro planeta. Los valores y significados que se han dado al dolor a lo largo del tiempo han estado sujetos a una gran variabilidad, por ello no es de extrañar que su concepto, su interpretación, la forma de afrontarlo, su clasificación y también su tratamiento hayan presentado muy distintos matices, variando desde la componente mágica y sobrenatural hasta la médico-científica.
El dolor físico está considerado como una señal de alerta o como un complejo proceso de defensa indicativo de que algo no funciona como debiera, sin embargo, su percepción sensitiva es subjetiva y se asocia a una componente emocional, siendo es un síntoma asociado a numerosas enfermedades que afecta de forma negativa, en menor o mayor grado en la calidad de vida del paciente.
Escala visual analógica del dolor
La Escala Visual Analógica (EVA) es una herramienta que se usa para ayudar a una persona a evaluar la intensidad de ciertas sensaciones y sentimientos, como el dolor. La escala visual analógica para el dolor es una línea recta en la que un extremo significa ausencia de dolor y el otro extremo significa el peor dolor que se pueda imaginar. El paciente marca un punto en la línea que coincide con la cantidad de dolor que siente. Se puede usar para elegir la dosis correcta de un analgésico.
La valoración será:
1 Dolor leve si el paciente puntúa el dolor como menor de 3.
2 Dolor moderado si la valoración se sitúa entre 4 y 7.
3 Dolor severo si la valoración es igual o superior a 8.
Las úlceras venosas suponen un problema de salud para el paciente muy importante afectando además a una parte de las personas mayores de 65 años. Independientemente a la edad, las ulceras suponen repercusiones a nivel biopsicosocial; ya que implica complicaciones como dolor continuado, soportar mal olor desprendido por la propia herida, tener limitaciones funcionales para poder deambular y posibles problemas de adherencia terapéutica. Es decir, no solo está afectada una parte anatómica, sino una persona en su conjunto, que terminarán o terminan afectando a la persona a nivel físico, funcional, emocional, social, laboral e incluso a nivel de realización personal.
La cura de las úlceras venosas crónicas (UVC) suele ser un procedimiento terapéutico difícil de realizar de manera completa y eficaz debido al dolor asociado a la cura, y los pacientes suelen requerir analgésicos orales para el tratamiento del dolor.
Como sabemos el desbridamiento mecánico acelera el proceso de curación mediante la eliminación de la fibrina y / o la necrosis, promueve la curación de las úlceras arteriales y venosas de las piernas, pero está limitado por el dolor asociado con el procedimiento.
En nuestros centros encontramos en una primera visita un perfil de paciente anímicamente deprimido, por los factores biopsicosociales alterados por la cronicidad de sus lesiones. En la mayoría de los pacientes, acudir a curas supone un proceso traumático, ya que presuponen que van a sentir más dolor del que soportan a lo largo del día, las 24 horas del día. Por ello, una de nuestras premisas principales, además de la curación, es el alivio del dolor, mediante un manejo efectivo de la úlcera. Como hemos mencionado anteriormente, el desbridamiento es una de las principales claves en el tratamiento, por ello intentaremos realizarlo con el mínimo dolor posible.
¿Qué son los anestésicos locales para curas sin dolor?
Los anestésicos locales son fármacos capaces de bloquear de manera reversible la conducción del impulso nervioso en cualquier parte del sistema, lo que da lugar a una pérdida de sensibilidad, aunque la función nerviosa se recupera completamente una finalizado su efecto.
Estructuralmente, las moléculas de los actuales anestésicos locales están integradas por tres elementos básicos:
- Un grupo hidrofóbico: un anillo aromático, determinante de la liposolubilidad, difusión y fijación de la molécula. La liposolubilidad del fármaco determina la potencia farmacológica: a mayor liposolubilidad mayor potencia.
- Un grupo hidrofílico: una amina secundaria o terciaria, que modula la hidrosolubilidad y por consiguiente su difusión sanguínea e ionización.
- Una cadena intermedia con un enlace de tipo éster o amida, responsable de la velocidad de metabolización del fármaco y, por tanto, determinante de la duración de la acción y su toxicidad.
Los anestésicos locales son fármacos que logran una pérdida de sensibilidad localizada y restringida, sin inducir una pérdida de conciencia ni del control central de las funciones vitales. Estos fármacos tienen como principal objetivo es suprimir de la sensación dolorosa, es decir los impulsos nociceptivos.
Su utilidad en la práctica clínica es amplia y depende de la vía de administración, de la técnica anestésica utilizada y de distintas indicaciones.
No existe en la actualidad ningún anestésico que reúna todos los requisitos para ser útil y seguro en cualquier situación clínica, por lo cual deberá elegirse el anestésico más adecuado para cada tipo de intervención y paciente.
Por ello realizamos una entrada mediante búsquedas bibliográficas sobre la aplicación de anestésicos locales que, además incluimos en nuestro protocolo de curación.
Los anestésicos en crema para curas sin dolor
Lambdalina LAMBDALINA 40 mg/g crema
Contiene lidocaína y es un medicamento que induce la pérdida de sensibilidad local (anestesia local) de la piel, ideal para las curas sin dolor.
Se usa para desensibilizar la piel en relación a la inserción de agujas, pero está contraindicada para apliacarla en deterioro de la integridad cutánea.
Curacaine La crema de lidocaína 4%
Es un anestésico local que ayuda a reducir el dolor durante cualquier procedimiento con aguja, como la colocación de una vía intravenosa, una inyección o durante una extracción sanguínea. Si además de aplicar esta crema se coloca al paciente en una posición cómoda y se le distrae, se reducirá el dolor o la molestia durante el procedimiento. Para una mayor eficacia, debe aplicarse y permanecer en la piel de 20 a 30 minutos antes del procedimiento. Se puede dejar hasta 2 horas. Pero está contraindicada en deterioro de la integridad cutánea.
LMX4
Es una crema anestésica tópica que contiene un anestésico llamado lidocaína al 4%, una concentración de venta libre. Está indicado para su uso como analgesia local para reducir el dolor y las molestias provocadas por las irritaciones de la piel. Pero está contraindicada en deterioro de la integridad cutánea, por lo que complica las curas sin dolor en úlceras.
Emla para curas sin dolor
Contiene 1 g de crema contiene 25 mg de lidocaína y 25 mg de prilocaína, indicada en punciones o intervenciones quirúrgicas superficiales tanto en adultos y en población pediátrica. Anestesia tópica de la mucosa genital, por ejemplo, antes de intervenciones quirúrgicas superficiales o de anestesia por infiltración; en adultos y adolescentes ≥12 años, además de estar indicada como anestesia tópica de úlceras en extremidades inferiores, para facilitar la limpieza mecánica/desbridamiento sólo en adultos.
El sevoflurano es un anestésico derivado halogenado del éter dietílico que se presenta como un líquido volátil. Es ampliamente utilizado por vía inhalatoria para la inducción y el mantenimiento de la anestesia general, pues su perfil de seguridad es muy bueno.
Además de su acción hipnótica, diversas experiencias preclínicas muestran que el sevoflurano y otros derivados halogenados del éter producen un efecto analgésico/anestésico importante cuando son administrados en su formulación líquida directamente al sistema nervioso central, concretamente a la médula espinal, pero clásicamente se les considera carentes de efecto analgésico a nivel periférico.
Sin embargo, en los últimos años se están comunicando experiencias clínicas en las que el sevoflurano produce un efecto analgésico importante sobre heridas dolorosas cuando es irrigado en su presentación líquida sobre el lecho de dichas heridas. Este efecto analgésico se caracteriza por instaurarse en escasos minutos, ser lo bastante intenso como para permitir el desbridamiento mecánico de las heridas, y extenderse por espacio de varias horas. Mejora la cicatrización de las heridas posiblemente debidas a un efecto vasodilatador, antiinflamatorio y analgésico.
Hasta ahora no ha sido comunicado efectos adversos a nivel sistémico, Puede causar efectos adversos locales leves y autolimitados como es el prurito leve y transitorio.
Sevoflurano necesita de más estudios experimentales para encontrar respuestas sobre tipos de heridas a emplearlo, frecuencia de aplicación, dosis para que sea optimo, así como la seguridad para el profesional a la hora de su uso.
Gel de morfina tópico para curas sin dolor
Es importante destacar que no existe actualmente una formulación tópica a base de opioides comercialmente disponible, sino que estas son prescritas y administradas a partir de formulaciones magistrales particulares.
Los principales opioides estudiados en este sentido son morfina, metadona, diamorfina y buprenorfina.
Se basa generalmente en la realización de fórmula magistral de morfina al 0.1% con un hidrogel conductor ya que la morfina clorhidrato es un principio activo hidrosoluble acido compatible con el hidrogel, que da viscosidad y estabilidad al preparado y actúa de vehículo para la absorción.
La evidencia científica disponible sobre la eficacia clínica del uso de opioides tópicos es escasa y heterogénea, sobre todo para curas sin dolor.
En la mayoría de pacientes se obtiene una anestesia suficiente para la limpieza de las úlceras de extremidades inferiores con un tiempo de aplicación de 30 minutos. Un tiempo de aplicación de 60 minutos puede mejorar la anestesia. El procedimiento de limpieza se debe iniciar antes de que transcurran 10 minutos después de retirar la crema.
Habitualmente aplicamos la crema en capa gruesa sobre la herida, cubrimos con un apósito oclusivo y lo retiramos a los 30 minutos, momento en el que se consigue el efecto anestésico que va a facilitar la manipulación de la herida durante la cura. De igual modo la crema puede aplicarse para quemaduras de 2º grado que se absorbe por vía percutánea siendo de eficacia analgésica.
Esta crema está constituida por una mezcla de lidocaína 2,5% y prilocaína 2,5% (LPC) se aplica sobre la herida y posteriormente se cubre con un apósito oclusivo no transpirable para favorecer su difusión hasta las terminaciones nerviosas. La dosis recomendada es de 1-2 gr/10 cm2, hasta un máximo de 10 gr, con un tiempo de latencia de 30-60 minutos. El efecto analgésico en las úlceras puede durar hasta 4 horas aproximadamente, y presenta una absorción sistémica lenta por la disminución del retorno venoso. La intensidad y la calidad del efecto anestésico dependen del tiempo de aplicación, la dosis aplicada y las características de la úlcera. Los autores añaden que este fármaco, en comparación con placebo, puede reducir el número de sesiones de limpieza requeridos para conseguir una úlcera limpia, que los tratamientos repetidos con esta crema no modifican de manera significativa la flora bacteriana de la úlcera, y raramente causan sensibilización.
EMLA produce una respuesta vascular bifásica que empieza con una vasoconstricción seguida de una vasodilatación en la zona de aplicación.
La crema EMLA es un fármaco seguro, aunque pueden aparecer reacciones locales, como enrojecimiento o palidez. No se ha detectado una influencia negativa en el proceso de cicatrización e, incluso, se ha descrito un potencial papel antiinflamatorio y antibacteriano. Si se excede la dosis recomendada, existe un potencial riesgo de desarrollar cardiotoxicidad, neurotoxicidad o metahemoglobinemia, esta última derivada de la capacidad de los metabolitos de la prilocaína de oxidar la hemoglobina, que se vuelve incapaz de transportar el oxígeno. La aplicación diaria de 10 g de EMLA (dosis máxima recomendada) durante 60 minutos al día,10 días, parece no tener efecto acumulativo en plasma y el pico de concentración máxima alcanzado es inferior al 40% de la concentración asociada con toxicidad.
Eliminación/absorción; Las concentraciones plasmáticas tras el tratamiento con EMLA son 20-60% inferiores para la prilocaína que, para la lidocaína, debido al mayor volumen de distribución y a una eliminación más rápida. La principal vía de eliminación de la lidocaína y la prilocaína es mediante el metabolismo hepático y los metabolitos se excretan por vía renal. Sin embargo, la tasa de metabolismo y eliminación de los anestésicos locales tras la aplicación tópica de EMLA vienen determinadas por la tasa de absorción. Por consiguiente, una reducción de la eliminación, como en los pacientes con insuficiencia en la función hepática, tiene efectos limitados sobre las concentraciones plasmáticas sistémicas después de una dosis única de EMLA y después de dosis únicas repetidas una vez al día a corto plazo (hasta 10 días).
Discusión sobre el tratamiento del dolor para la cura de úlceras
Sobre el tratamiento tópico del dolor durante el cuidado de úlceras venosas, indica que actualmente la crema de lidocaína-prilocaína al 5% es el único anestésico tópico aprobado con indicación para el desbridamiento y/o la limpieza de heridas en las extremidades inferiores.
evaluaron el efecto de una crema lidocaína-prilocaína para aliviar el dolor asociado con el desbridamiento de la úlcera. La diferencia entre los grupos en cuanto al dolor, medido en una escala visual de 100 mm, fue estadísticamente significativa a favor de la crema de lidocaína-prilocaína.
La evidencia sugiere que los apósitos de ibuprofeno pueden ofrecer alivio del dolor a las personas con úlceras venosas dolorosas en las piernas y que la crema lidocaína-prilocaína parece proporcionar un alivio efectivo del dolor durante el desbridamiento de las úlceras venosas de las piernas.
También hemos encontrado un estudio donde compararan el efecto de la crema de lidocaína-prilocaína al 5% con una solución de odontología en aerosol de lidocaína al 10, para reducir el dolor durante el desbridamiento quirúrgico en las úlceras venosas de las piernas. En este estudio se mostró que los pacientes tratados con aerosol tomaron más analgésicos, pero, por otra parte, la aplicación del aerosol redujo el tiempo del procedimiento y mejoró el cumplimiento del paciente. El autor concluye que para el desbridamiento rápido, lo más apropiado es usar anestésico en aerosol.
En relación al gel de morfina tópico las dos series de casos coinciden en que todos los pacientes experimentaron una reducción significativa del dolor con el uso del gel tópico de morfina y no percibieron efectos secundarios. Solo un caso de uno de los estudios tuvo una respuesta ambigua y los autores indican que pudiera ser un candidato inadecuado al tratamiento, debido a que la úlcera no era abierta.
Según la guía clínica del manejo del dolor durante las curas de pie diabético, escaras y heridas post quirúrgicas en Atención Primaria, realizan analgesia previa a la curación con los siguientes métodos de analgesia local:
- Depositar lidocaína al 2% o gel de lidocaina 1/2h antes de la cura.
- Depositar morfina/gel de morfina en apósitos que cubran la herida 1/2h antes de la cura.
- Cubrir con pomada anestésica de lidocaína y prilocaína (EMLA®), 1 hora antes de la cura aproximadamente, y cubriéndola con un apósito oclusivo. Según experiencia de los autores, con media hora es suficiente para obtener un nivel adecuado de analgesia.
Es importante destacar algunos artículos encontrados en los que se destaca una disminución de la infección en los casos en los que se aplica lidocaína.
Aún no es posible eliminar por completo el riesgo de infección, pero sí es posible su reducción hasta un nivel mínimo y poder ofrecer un beneficio al paciente, disminuir los recursos utilizados, siendo el objetivo principal de este estudio la disminución del desarrollo de infección en heridas limpias-contaminadas y contaminadas, al aplicar lidocaína simple al 2% en el tejido celular subcutáneo al término de la cirugía.
Conclusiones sobre las curas sin dolor
Bajo oclusión, la crema EMLA reduce significativamente el dolor del desbridamiento agudo, disminuye la incidencia de dolor posterior al desbridamiento y reduce el tiempo necesario para lograr una limpieza. Las dosis de hasta 10 g de EMLA dan como resultado niveles plasmáticos de lidocaína y prilocaína muy por debajo de los niveles tóxicos. El tratamiento repetido no modifica la flora bacteriana de la úlcera y rara vez provoca sensibilización.
EMLA sigue siendo el anestésico tópico más utilizado dada su eficacia y seguridad probadas en varios ensayos clínicos. Ha habido una liberación reciente de varios agentes anestésicos tópicos nuevos con cierta eficacia demostrada después de un tiempo de aplicación de 30 minutos. Se coloca y almacena un depósito de anestésico en las capas superiores de la piel durante la aplicación, lo que proporciona un beneficio anestésico adicional 30 minutos después de la extracción.
¡QUEREMOS CURAR Y CURAR SIN DOLOR!
Bibliografía de curas sin dolor
- Bonet R. Anestésicos locales. Offarm. 1 de septiembre de 2011;30(5):42-7.
- Definición de EVA – Diccionario de cáncer del NCI – Instituto Nacional del Cáncer [Internet]. 2011 [citado 16 de diciembre de 2021]. Disponible en: https://www.cancer.gov/espanol/publicaciones/diccionarios/diccionario-cancer/def/eva
- Marrero González CM, Marrero González CM. Repercusiones de padecer una Úlcera Venosa. Ene [Internet]. 2020 [citado 8 de diciembre de 2021];14(2). Disponible en: https://scielo.isciii.es/scielo.php?script=sci_abstract&pid=S1988-348X2020000200014&lng=es&nrm=iso&tlng=en
- Tratamiento del dolor en úlceras venosas crónicas – ClinicalKey [Internet]. [citado 8 de diciembre de 2021]. Disponible en: https://www.clinicalkey.es/#!/content/journal/1-s2.0-S0213925117301491
- PROSPECTO LAMBDALINA 40 mg/g CREMA [Internet]. [citado 16 de diciembre de 2021]. Disponible en: https://cima.aemps.es/cima/dochtml/p/69789/Prospecto_69789.html
- _ApplicationFrame [Internet]. Children’s Minnesota. [citado 16 de diciembre de 2021]. Disponible en: http://www.childrensmn.org/educationmaterials/childrensmn/article/16945/crema-anestesica-lmx4r-curacainer/
- LMX4 Topical Anesthetic Cream [Internet]. Eloquest Healthcare, Inc. [citado 16 de diciembre de 2021]. Disponible en: https://eloquesthealthcare.com/lmx4/
- ★ LMX4 Cream 4% de Reino Unido 🥇 [Internet]. [citado 16 de diciembre de 2021]. Disponible en: https://www.vademecum.es/equivalencia-lista-lmx4+cream+4%25-reino+unido-d04ab01-31016044-gb_1
- Gerónimo-Pardo M, Cortiñas-Sáenz M, Gerónimo-Pardo M, Cortiñas-Sáenz M. Eficacia analgésica del sevoflurano tópico en heridas. Rev Soc Esp Dolor. abril de 2018;25(2):106-11.
- Imbernón Moya A, Imbernón Moya A. Valoración del dolor, satisfacción, impacto en la calidad de vida y capacidad funcional con la administración de sevoflurano tópico previo a la curación de úlcera venosa crónica [Internet]. Universidad Complutense de Madrid; 2018 [citado 16 de diciembre de 2021]. Disponible en: https://eprints.ucm.es/id/eprint/50297/
- Conde E. ¿Habías oído hablar del uso tópico del sevoflurano en heridas? [Internet]. Elena Conde Montero. 2017 [citado 16 de diciembre de 2021]. Disponible en: https://www.elenaconde.com/habias-oido-hablar-del-uso-topico-del-sevoflurano-en-heridas/
- Bastami S, Frödin T, Ahlner J, Uppugunduri S. Topical morphine gel in the treatment of painful leg ulcers, a double-blind, placebo-controlled clinical trial: a pilot study. Int Wound J. agosto de 2012;9(4):419-27.
- FICHA TECNICA EMLA 25 mg/g + 25 mg/g CREMA [Internet]. [citado 8 de diciembre de 2021]. Disponible en: https://cima.aemps.es/cima/dochtml/ft/61096/FT_61096.html
- Conde E. ¿EMLA como apósito primario en las heridas dolorosas? Sí [Internet]. Elena Conde Montero. 2017 [citado 8 de diciembre de 2021]. Disponible en: https://www.elenaconde.com/emla-como-aposito-primario-en-las-heridas-dolorosas-si/
- Lillieborg S, Aanderud L. EMLA anaesthetic cream for debridement of burns: a study of plasma concentrations of lidocaine and prilocaine and a review of the literature. Int J Burns Trauma. 2017;7(6):88-97.
- Vanscheidt W, Sadjadi Z, Lillieborg S. EMLA anaesthetic cream for sharp leg ulcer debridement: a review of the clinical evidence for analgesic efficacy and tolerability. Eur J Dermatol EJD. abril de 2001;11(2):90-6.
- Effendy I, Gelber A, Lehmann P, Huledal G, Lillieborg S. Plasma concentrations and analgesic efficacy of lidocaine and prilocaine in leg ulcer-related pain during daily application of lidocaine-prilocaine cream (EMLATM) for 10 days. Br J Dermatol. julio de 2015;173(1):259-61.
- Murcia C de S de la R de. Lidocaína al 2% para reducir el dolor en el cuidado de úlceras venosas. / 2% lidocaine to reduce pain when caring for venous ulcers. [Internet]. [citado 8 de diciembre de 2021]. Disponible en: http://www.murciasalud.es/preevid/23624
- EMLA and Lidocaine Spray: A Comparison for Surgical Debridement in Venous Leg Ulcers | Advances in Wound Care [Internet]. [citado 8 de diciembre de 2021]. Disponible en: https://www.liebertpub.com/doi/10.1089/wound.2014.0605
- Claeys A, Gaudy-Marqueste C, Pauly V, Pelletier F, Truchetet F, Boye T, et al. Management of pain associated with debridement of leg ulcers: a randomized, multicentre, pilot study comparing nitrous oxide–oxygen mixture inhalation and lidocaïne–prilocaïne cream. J Eur Acad Dermatol Venereol. 2011;25(2):138-44.
- Preevid SM de S. Banco de preguntas Preeevid. Manejo del dolor durante las curas de pie diabético, escaras y heridas post quirúrgicas en Atención Primaria. [Internet]. Preevid. Servicio Murciano de Salud. Region de Murcia; 2013. Disponible en: http://www.murciasalud.es/preevid.php?op=mostrar_pregunta&id=19583
- Noriega-Salas AL, Sánchez-López-López MÁ, Esperón Lorenzana GI, Trejo Suárez J. Aplicación de lidocaína simple al 2% en tejido celular subcutáneo de heridas quirúrgicas limpias-contaminadas y contaminadas para disminuir la incidencia de infección. Cir Gen. septiembre de 2011;33(3):180-4.
- Friedman PM, Mafong EA, Friedman ES, Geronemus RG. Topical anesthetics update: EMLA and beyond. Dermatol Surg Off Publ Am Soc Dermatol Surg Al. diciembre de 2001;27(12):1019-26.
Quizás te interese

Con el frío invernal aumentan los sabañones (perniosis). Hoy te explicamos qué son, por qué ocurren, quién tiene más riesgo, cómo prevenirlos y cuál es su tratamiento, tal y como recoge la literatura citada.
Índice
El frío y los sabañones
Con la llegada del invierno y la notable bajada de temperaturas de este año, aparecen problemas como la perniosis, más conocida como sabañones, provocados por el frío.
¿Qué es un sabañón?
Los sabañones son una inflamación dolorosa de pequeños vasos cutáneos que surge tras exposición repetida al aire frío (no helado). También llamados eritema pernio, pueden producir picor, manchas rojas, hinchazón y ampollas en manos y pies. Son más frecuentes desde finales de otoño hasta inicios de primavera, especialmente en invierno, y pueden afectar manos, pies, dedos, orejas o nariz.
Se distinguen dos formas: idiopática (sin enfermedad sistémica asociada) y secundaria (vinculada a diversos trastornos, principalmente lupus eritematoso).
Epidemiología
El eritema pernio es común en países con clima frío o templado y húmedo con invierno marcado (por ejemplo, Gran Bretaña, Francia o la costa norte de EE. UU.). Se observa con mayor frecuencia en mujeres jóvenes (15–30 años), aunque también aparece en niños y ancianos.
Clínica
Signos y síntomas habituales:
-
Pequeñas áreas enrojecidas pruriginosas, sobre todo en pies o manos.
-
Ampollas o úlceras posibles.
-
Edema cutáneo.
-
Sensación de ardor.
-
Cambios de color de rojo a azul oscuro con dolor.
Las lesiones pueden ser únicas o múltiples, a menudo simétricas y bilaterales, y adoptar forma de máculas, pápulas, placas o nódulos eritemato-violáceos sobre base edematosa; pueden ampollarse y ulcerarse, sin síntomas sistémicos.
Histología: edema en dermis papilar e infiltrado inflamatorio linfocitario perivascular superficial y/o profundo.
Eritema pernio primario (idiopático):
-
Agudo: aparece en piel sin vello a las 12–24 h tras ambiente frío y húmedo. Lesiones únicas o múltiples, simétricas y bilaterales; pápulas, máculo-placas o placas eritematosas/violáceas/parduzcas/amarillentas sobre base fría y edematosa, a veces descamativas, con posibilidad de ampollas y úlceras.
-
Crónico: tras exposición repetida al frío, con persistencia de las lesiones, cicatrización y atrofia; puede mantenerse tras la temporada fría o reaparecer con nuevas exposiciones (ese invierno o en años siguientes). Posibles cambios irreversibles: fibrosis, linfedema e hiperqueratosis.
Variantes clínicas:
-
Perniosis ecuestre (paniculitis ecuestre por frío): en glúteos y caderas de mujeres que cabalgan en invierno; pápulas/placas agrupadas que pueden ulcerarse.
-
Manos de frotador: combinación de aire húmedo y frío con trauma por frotado vigoroso en clima frío.
-
Perniosis papular: pequeñas lesiones agrupadas en caras laterales de dedos, a menudo con acrocianosis; clínicamente recuerda al eritema multiforme, sin sus cambios histológicos, y puede surgir todo el año.
-
Pernio inducido por fármacos: descrito con análogos de anfetaminas como fenfluramina y fentermina (adelgazantes).
-
Perniosis senil: lesiones más persistentes y, por lo general, con enfermedad arterial o sistémica de base.
¿Por qué se produce? Causas
La causa exacta no se conoce. El frío puede desencadenar perniosis en unos individuos y no en otros; puede aparecer de forma aislada en personas sanas o en el contexto de otras enfermedades.
Se han propuesto mecanismos como una respuesta anómala al frío con regulación deficiente del flujo cutáneo: vasoconstricción persistente de arteriolas profundas y dilatación de vasos superficiales (en lugar de la vasodilatación de rebote que mantendría la perfusión). La exposición al frío provoca vasoconstricción masiva y descenso de la temperatura cutánea (protege la temperatura central a costa de la piel).
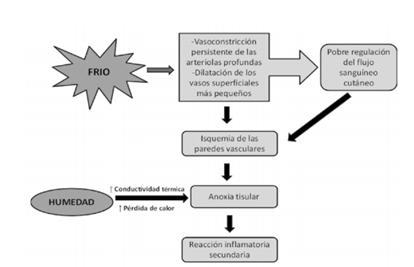
La temperatura cutánea normal (≈ 33–35 °C) al caer por debajo de 31 °C induce vasoconstricción de arteriolas y vénulas, empeorando la conductividad térmica y aumentando la
La temperatura cutánea normal es de 33-35 °C que cuando cae a 31 °C o menos provoca la vasoconstricción de las arteriolas y las vénulas, que empeora la conductividad térmica y aumenta la pérdida de calor y la resistencia a la congelación cuando la piel está húmeda. El trauma inducido por frío produce daño vascular por la anoxia tisular, provocando una reacción inflamatoria secundaria.
La naturaleza y magnitud de la perniosis, al igual que otras lesiones por frío, dependen de la interacción entre el clima, las medidas protectoras y la producción metabólica de calor, así como otros factores como la edad, la raza, el sexo femenino, la malnutrición, un índice bajo de masa corporal, entre otros.
En definitiva, es una reacción anormal del cuerpo a la exposición al frío, seguida de recalentamiento; de forma que cuando se vuelve a calentar la piel fría, los vasos sanguíneos pequeños debajo de la piel pueden expandirse más rápido de lo que pueden soportar los vasos cercanos más grandes. Esto produce un efecto de cuello de botella y pérdida de sangre hacia los tejidos cercanos.
Factores de riesgo o predisponentes.(1–4)
Los factores que pueden aumentar el riesgo de padecer sabañones son:
- El uso de ropa ajustada o que expone la piel al frío.Usar ropa y calzado ajustado en climas fríos y húmedos puede volverte más susceptible a los sabañones.
- El sexo.Las mujeres son más propensas a padecer sabañones que los hombres.
- Pieles frías y húmedas; son mas propensas a la aparición de sabañones.
- Estar por debajo del peso apropiado.Las personas que pesan cerca del 20 % menos de lo que debería según su altura tienen un mayor riesgo de padecer sabañones.
- El ambiente y la estación.Los sabañones son menos frecuentes en zonas más frías y secas porque las condiciones de vida y la ropa que se utiliza en estas zonas protegen más del frío. El riesgo es mayor en zonas de humedad alta y temperaturas frías, pero no heladas.
- Tener mala circulación como una insuficiencia venosa crónica o Enfermedad periférica arterial.Las personas con mala circulación tienden a ser más sensibles a los cambios en la temperatura, lo que las hace más susceptibles a los sabañones, debiendo tener especial atención al curso y tratamiento del sabañón ya que pueden desencadenar en una herida o úlcera.
- Padecer la enfermedad de Raynaud.Las personas con la enfermedad de Raynaud son más susceptibles a los sabañones que pueden llegar a camuflarse ya que la enfermedad de Raynaud causa diferentes tipos de cambios de color en la piel.
- Padecer un trastorno autoinmune como por ejemplo el lupus; una enfermedad del tejido conectivo siendo el trastorno autoinmune más frecuente asociado a los sabañones, asi como otras enfermedades como la Artrosis, Artritis Reumatoide etc
- Especial atención en pacientes que sufren de diabetes Mellitus, neuropatía diabética, Ya que la sensibilidad en Miembros inferiores esta disminuida por lo que la sensación de dolor no es captada por el paciente. Por ello es recomendable la inspección de los pies diarias y ante cualquier alteración acudir a consulta de podología o enfermería para la vigilancia y los cuidados necesarios.
- Con frecuencia afecta en mayor medida a las mujeres que a los varones. A menudo también existe una predisposición familiar a desarrollar lesiones idénticas, sobre todo durante la adolescencia y en los adultos jóvenes.
Complicaciones.(1,4,5)
Por lo general, los sabañones mejoran por sí solos. Busca atención para vigilar y controlar la evolución si surgen complicaciones como:
- Dolor es excepcionalmente intenso.
- Si se sospecha que puedes tener una infección o si los síntomas no mejoran después de 1 o 2 semanas.
- Si los síntomas continúan durante la temporada más cálida, consulta con el médico para descartar otras afecciones.
- Si tienes diabetes o mala circulación, es posible que la curación se vea afectada. Ten cuidado y busca atención especializada.
Los sabañones pueden causar complicaciones si la piel se ampolla. Si eso sucede, es posible que tengas úlceras e infecciones. Además de ser dolorosas, las infecciones podrían poner en riesgo la extremidad o la vida si no se tratan.
Prevención. (1–4)
- Evitar o limitar la exposición al frío.
- Vestirse con varias capas de ropa suelta, y usa guantes y calzado abrigado e impermeable.
- Cubrir lo posible toda la piel expuesta cuando salgas al exterior los días de frío.
- Mantener las manos, los pies, y la cara secos y abrigados.
- Mantener la casa y/o lugar de trabajo a una temperatura cálida agradable.
- Calentar la piel expuesta al frío gradualmente, ya que calentarla de manera repentina la piel fría puede empeorar los sabañones.
- Evitar el tabaco.
Tratamiento.(2–5)
El protocolo de tratamiento inicialmente se va a basar en tomar una serie de medidas que son básicas y un tanto generales.
Estas medidas básicas se van a centrar en proteger la zona lesionada siempre secas y calientes. Para ello el paciente debe hacer uso de guantes y de unos calcetines adecuados.
El tratamiento domiciliario se basa en la aplicación de crema hidro regenerante para prevenir y tratar los sabañones, con componentes como:
- productos ozonizados; entre sus funciones destaca:
- Aumenta la elasticidad.
- Altamente emoliente (alisa y suaviza la piel).
- Evita la aparición de manchas.
- Frena la deshidratación.
- Caléndula;
- Cicatrizante.
- Antiinflamatorio.
- Antiséptico.
- Urea; aumenta la capacidad de hidratación de la piel.
- Centella asiática; acelera la cicatrización.
- Extracto glicólico de manzanilla; contiene alfa-bisabolol con propiedades:
- Antiinflamatorias.
- Calmantes.
- Cicatrizantes.
En definitiva, como prevención y tratamiento es recomendable el uso de una crema de alto poder hidratante y regenerador, que nutra, calme y regenere las pieles irritadas que esté especialmente indicada para manos y/o pies estropeados.
Pero si estas recomendaciones básicas y tratamiento tópico domiciliario no tienen un resultado positivo debemos tratarlos de manera interna, es decir, con tratamientos farmacológicos como la pentoxifilina, la hidrocloroquina y la nitroglicerina tópica parecen ser beneficiosos para el tratamiento de la perniosis crónica, aunque el tratamiento local más común es la betametasona tópica. Estos tratamientos farmacológicos, por un lado, van a aumentar la presión del paciente, del mismo modo el paciente va a ver mejoría en su circulación sanguínea, y, por último, este tratamiento va a favorecer la dilatación de los vasos sanguíneos.
El sabañón causa inflamación, dolor y sensación de quemazón. A veces, puede llegar a producirse necrosis o a surgir pequeñas úlceras. En tal caso habría que hacer un tratamiento con corticoides tópicos o incluso con antibióticos para evitar la sobreinfección.
Desde CMUC os damos unas recomendaciones básicas:
- Evitar la exposición al frío.
- Realizar ejercicio físico con regularidad.
- Usar ropa aislante adecuada.
- Prescindir del tabaco.
- Incrementar la ingesta de alimentos con vitaminas A ya que ayudan a restaurar los tejidos dañados. Para proteger los capilares sanguíneos puedes añadir a tu dieta alimentos ricos en Vitamina C como el kiwi, la naranja, el limón o el brécol.
- Incluye en la dieta especies tales como la cayena, la canela o la pimienta. Cocinar con estos condimentos ayuda a tu circulación, ya que son alimentos vasodilatadores.
- Toma alimentos ricos en Vitamina E, como por ejemplo el aguacate, el brócoli o las espinacas. Estos alimentos ayudan a mejorar el riego sanguíneo.
- Consumir alimentos ricos en vitamina D, estimulan la circulación.
- Masajear las zonas propensas para estimular el flujo sanguíneo.
- Aplicar cremas hidratantes que palíen la sequedad de la piel.
- No exponer las manos ni los pies directamente a la estufa o al radiador pues los cambios bruscos de temperatura aumentan el riesgo de que se generen.
Pero recuerda evitar las verduras de hoja ancha ricas en vitamina K, como por ejemplo las acelgas, lechuga o espinacas, ya que su ingesta no es recomendable más de una vez en semana, porque no favorecen la insuficiencia venosa crónica o si estás en tratamiento con Sintrom o anticoagulantes debido a su acción directa sobre la coagulación en sangre.
Bibliografía.
- Sabañones – Síntomas y causas – Mayo Clinic [Internet]. [citado 30 de diciembre de 2020]. Disponible en: https://www.mayoclinic.org/es-es/diseases-conditions/chilblains/symptoms-causes/syc-20351097
- Bielsa Marsol I. Perniosis. Semin Fund Esp Reumatol. 1 de abril de 2012;13(2):55-61.
- Baker JS, Miranpuri S. Perniosis A Case Report with Literature Review. J Am Podiatr Med Assoc. marzo de 2016;106(2):138-40.
- Tobón MX, Rodríguez G. Eritema pernio: una enfermedad misteriosa. 2013;(1):14.
- Pie IV del. ▷ ¿Qué son los sabañones? Síntomas, causas y tratamiento 🔥 [Internet]. Instituto Valenciano del Pie. 2019 [citado 30 de diciembre de 2020]. Disponible en: https://institutovalencianodelpie.es/sabanones-sintomas-y-tratamiento/
Divulgación
Insuficiencia Arterial: Qué es, causas, síntomas y tratamientos
Publicado
hace 2 mesesel
3 de diciembre de 2025
Este artículo es una inmersión profunda en la patología vascular, explicaremos qué es la insuficiencia arterial, sus causas síntomas y tratamientos. Ideal para pacientes o profesionales que busquen entender sus síntomas y las opciones de diagnóstico disponibles.
Índice
¿Qué es una arteria y cómo funciona?
La palabra “arteria” proviene del griego ἀρτηρία, que significa “tubo, conducción”. La arteria es el vaso sanguíneo encargado de distribuir la sangre expulsada de las cavidades ventriculares del corazón en cada sístole al resto del organismo y lecho capilar.
Sus paredes son muy resistentes y elásticas para resistir la presión que ejerce la sangre al salir bombeada del corazón. Cada vaso arterial consta de tres capas concéntricas:
-
Interna o íntima: constituida por el endotelio.
-
Media: capa gruesa compuesta por fibras musculares lisas, fibras elásticas y de colágeno.
-
Externa o adventicia: formada por tejido conjuntivo.
Los límites entre las tres capas están generalmente bien definidos en las arterias. Siempre presentan una lámina elástica interna separando la íntima de la media, y (a excepción de las arteriolas) presentan una lámina elástica externa que separa la media de la adventicia. La lámina externa se continúa menudo con las fibras elásticas de la adventicia.
Existen diferentes tipos arteriales:
- Arterias elásticas: Son los grandes vasos de conducción, la aorta, los troncos innominados, la carótida común y las subclavias. Sus paredes tienen una gran elasticidad, lo que permite hacer más regular el flujo sanguíneo. La capa media esta formada por una gran concentración de capas de elastina, además de células musculares lisas, fibras colágenas, proteoglicanos y glicoproteinas.
- Arterias musculares: Las principales ramas de distribución, la arteria radial, la arteria femoral, la arteria coronaria y la arteria cerebral (todas ellas importantes ramificaciones). La capa media importante es rica en fibras musculares lisas. Tienen una potente capa adventicia, rica en colágeno y fibras elásticas. Vasa vasorum, nervi vasorum que llegan a la porción más externa de la capa media.
- Arteriolas: Las ramas terminales que irrigan el territorio capilar. Tiene un tejido menos elástico y más presencia de fibras musculares lisas. La túnica adventicia es escasa.
- Microcirculación: se refiere al flujo de sangre de las arteriolas y capilares o los capilares y venas, es la parte del sistema circulatorio encargada del intercambio de gases, fluidos, nutrientes y productos de desecho.
Definición de Insuficiencia Arterial
La obstrucción arterial se caracteriza por la interrupción del flujo sanguíneo a una determinada parte de nuestro organismo como consecuencia de la oclusión crónica de la arteria que lo irriga. La disminución del flujo sanguíneo ocasiona un aporte insuficiente de oxígeno a las células del organismo , produciendo hipoperfusión, hipoxemia y necrosis si no es restablecida la circulación.
Causas y Factores de Riesgo
Existen varias causas que pueden provocar un estrechamiento de la arteria y disminuir el flujo sanguíneo:
-
Arterioesclerosis: Una placa que se acumula en las paredes de las arterias, compuesta por grasa y colesterol.
-
Trombosis: Un coágulo sanguíneo que se forma en un vaso y permanece allí.
-
Embolia: Coágulo que se desplaza desde el sitio donde se formó a otro lugar.
-
Calcificación vascular: Depósito de sales de fosfato de calcio en la pared de las arterias.
-
Otros: Hipertensión arterial, traumatismos o disección.
Entre los factores de riesgo más importantes implicados en el desarrollo de enfermedades vasculares y, por lo tanto de insuficiencia arterial están el tabaquismo, la diabetes mellitus, la hipertensión arterial sistémica, la dislipidemia, la edad y el sexo masculino.
Signos y Síntomas: ¿Cómo detectarlo?
La ubicación del dolor depende del lugar de la arteria obstruida o estrechada. Los signos más característicos incluyen:
-
Claudicación intermitente: Calambres dolorosos en caderas, muslos o pantorrillas después de realizar ciertas actividades, como caminar, que desaparecen después de algunos minutos de descanso.
-
Dolor en reposo isquémico: Si la enfermedad progresa, aparece dolor incluso estando acostado, lo suficientemente intenso como para interrumpir el sueño.
-
Cambios físicos: Entumecimiento, sensación de frío en la pierna o pie, pérdida de vello, crecimiento lento de las uñas, y piel brillante en las piernas.
-
Úlceras arteriales: Heridas que no sanan en los dedos de los pies, pies o piernas.

Diagnóstico de la Insuficiencia Arterial
Una adecuada anamnesis es necesaria para realizar un correcto diagnóstico. Para recabar datos disponemos de diferentes métodos:
-
Exploración física: Se palpan cuidadosamente los pulsos (femoral, poplíteo, tibial posterior y pedio). La ausencia de pulso tibial posterior es el mejor discriminador aislado de la isquemia crónica.
-
Índice Tobillo-Brazo (ITB): Fundamental para determinar el grado de afectación.
-
Angiografía: Se inyecta material de contraste para ver el flujo sanguíneo en tiempo real mediante radiografías, resonancia (ARM) o tomografía (ATC).
-
Análisis de sangre: Para medir colesterol, triglicéridos y presencia de diabetes.

Tratamientos Disponibles
El tratamiento empieza con la modificación de los factores de riesgo: dejar de fumar, realizar ejercicio (caminar en patrón ejercicio-descanso) y el control de diabetes/hipertensión.
Tratamientos Farmacológicos:
-
Antiagregantes plaquetarios (Aspirina, Clopidogrel).
-
Fármacos para la claudicación (Pentoxifilina, Cilostazol).
-
Inhibidores de la ECA.
Tratamientos Quirúrgicos:
-
Angioplastia: Uso de un balón para reabrir la arteria, a veces con colocación de stent.
-
Cirugía de bypass: Creación de un puente con un injerto para desviar la sangre alrededor de la obstrucción.
-
Tromboendarterectomía: Extirpación quirúrgica de la lesión oclusiva.
En pacientes con úlceras se procederá a la limpieza de estas. Si se ha conseguido la revascularización se realizarán desbridamientos amplios o incluso la amputación parcial (dedos de los pies) con el fin de evitar una sobreinfección de las heridas y conseguir una cicatrización final.
En caso de que la revascularización no funcione, se deberá proceder a la amputación parcial o total de la extremidad afectada, si existe un dolor no controlado o sobreinfección asociada.5
Se les aconseja a los pacientes que eviten el frío y los fármacos vasoconstrictores (por ejem. Seudoefedrina que forma parte de muchos remedios para la sinusitis y el resfriado).3
En CMUC ofrecemos a nuestros pacientes ozonoterapia como tratamiento para la curación de úlceras. El ozono tiene una gran capacidad oxidante que le confiere un importante poder contra bacterias, virus y hongos (este oxida la envoltura externa de bacterias y virus, destruyéndolos). También incrementa la circulación sanguínea, en especial la microcirculación (incrementa la liberación de oxígeno en los glóbulos rojos y así ceder el oxígeno a los tejidos periféricos).
Caso Clínico
Microinjertos Cutáneos – Casos Clínicos
Publicado
hace 2 mesesel
18 de noviembre de 2025Por
CMUC Admin
En el primer blog de esta serie de blogs sobre los microinjertos cutáneos, os explicamos los fundamentos de la técnica Hy-Tissue Micrograft (HT-MG): un procedimiento mínimamente invasivo que utiliza microfragmentos de piel autóloga para estimular la cicatrización en heridas crónicas cuando los tratamientos convencionales no han sido eficaces.
En este segundo artículo, nos centramos en la experiencia clínica recogida en el estudio: cinco pacientes con heridas de etiologías diversas tratados mediante HT-MG.
Se trata de un estudio analítico, observacional, transversal y prospectivo, para evaluar la eficacia clínica de esta técnica en términos de cierre de la herida, disminución del dolor y seguridad del procedimiento, manteniendo un enfoque práctico y reproducible en el entorno asistencial.
Índice
Perfil de los pacientes y características de las heridas
El estudio incluyó un total de cinco pacientes, seleccionados tras valorar que sus heridas no respondían de forma adecuada al tratamiento convencional con cura en ambiente húmedo (CAH).
La edad media fue de 63,8 años, con cuatro mujeres y un hombre, y una evolución media de las lesiones de dos años, lo que refleja la cronicidad de los casos. El tamaño medio de las heridas fue de 45,8 cm², con variaciones según la localización y etiología.
Las causas de las lesiones fueron variadas, lo que permitió observar la aplicación de la técnica en distintos contextos clínicos:
-
Enfermedad de Hansen
-
Dos úlceras venosas
-
Una lesión por dermatoporosis grado IV
-
Una úlcera neuropática plantar
Todas las heridas se encontraban limpias, sin signos de infección activa y con un lecho apto para la técnica HT-MG, cumpliendo los criterios establecidos para garantizar la viabilidad del injerto.
Los cinco casos incluidos en el estudio muestran la aplicación práctica de la técnica HT-MG en heridas de distinta etiología, con resultados globalmente positivos.
Caso 1 – Lesión por enfermedad de Hansen
Paciente diagnosticado de enfermedad de Hansen con una lesión cutánea crónica que no respondía al tratamiento convencional.
Tras aplicar el microinjerto autólogo mediante HT-MG, se observó una evolución progresiva hacia la cicatrización, con una reducción del tamaño de la herida hasta un residuo final de 2 × 2 cm al cierre del seguimiento.
Caso 2 – Úlcera venosa crónica
Paciente con úlcera venosa de larga evolución.
Tras la aplicación de HT-MG, se evidenció una mejoría rápida en el aspecto del lecho y una epitelización progresiva, alcanzando la cicatrización completa durante el periodo de seguimiento.
Caso 3 – Úlcera venosa crónica
Segundo caso de etiología venosa, con características clínicas similares al anterior.
El tratamiento con HT-MG permitió una evolución favorable, con formación de nuevo tejido epitelial y cierre completo de la lesión sin complicaciones.
Caso 4 – Dermatoporosis grado IV
Paciente con dermatoporosis avanzada (grado IV), que presentaba una lesión atrófica persistente.
La aplicación de microinjertos cutáneos favoreció una respuesta cicatricial notable, con cierre completo de la herida en las semanas posteriores y mejora del tejido circundante.
Caso 5 – Úlcera neuropática plantar
Caso de úlcera neuropática en la planta del pie, con evolución tórpida pese al manejo convencional.
El procedimiento HT-MG consiguió una epitelización completa sin signos de infección ni recidiva, lo que confirma su utilidad en este tipo de lesiones complejas.
Resultados generales y observaciones clínicas
Los resultados globales del estudio muestran una respuesta positiva en todos los casos tratados con microinjertos cutáneos HT-MG. La técnica permitió reducir los tiempos de cicatrización, disminuir el dolor y mejorar la calidad del tejido epitelial obtenido tras el cierre de las heridas.
El tiempo medio de cicatrización fue de aproximadamente 2,5 meses, con una evolución satisfactoria y sin necesidad de hospitalización. Ninguno de los pacientes presentó signos de colonización bacteriana ni infección local tras la aplicación.
El sitio donante (de donde se obtuvieron las biopsias de piel) mostró una recuperación completa entre los 7 y 15 días, sin complicaciones relevantes.
Además, se destacó la facilidad de aplicación del procedimiento, lo que sugiere que puede integrarse en el ámbito ambulatorio o en atención primaria, siempre que se cumplan los requisitos de asepsia, limpieza del lecho y estado general adecuado del paciente.
Consideraciones técnicas y biológicas
El éxito de la técnica se apoya en su base biológica: los microfragmentos obtenidos conservan la matriz extracelular (MEC), que actúa como soporte estructural y favorece la regeneración tisular al mantener nichos celulares activos y factores de crecimiento.
Desde el punto de vista mecánico, se hace referencia al principio de tensegridad, según el cual la estructura de la MEC mantiene la conexión entre las células y el entorno, facilitando su supervivencia e integración en el tejido receptor.
Conclusiones del estudio
El uso de microinjertos cutáneos autólogos (HT-MG) se presenta como una alternativa eficaz y mínimamente invasiva en el tratamiento de heridas crónicas que no responden a los métodos convencionales.
La técnica permite acortar los tiempos de cicatrización, reducir el dolor y obtener una cicatriz funcional y estéticamente aceptable, sin complicaciones infecciosas ni efectos secundarios relevantes.
Entre sus ventajas se encuentran:
-
Procedimiento ambulatorio, sin necesidad de hospitalización.
-
Recuperación rápida del sitio donante.
-
Aplicación sencilla y reproducible, adaptable al entorno de atención primaria o unidades de heridas.
No obstante, el éxito del tratamiento depende de una correcta selección del lecho, que debe estar bien irrigado y libre de tejido necrótico, fibrinoso o infectado.
La técnica no debe aplicarse directamente sobre hueso o tendón expuesto, ya que comprometería la viabilidad del injerto.
El trabajo demuestra que los microinjertos cutáneos HT-MG pueden ser una herramienta útil dentro del abordaje integral de las heridas complejas, especialmente cuando otras terapias no han logrado resultados satisfactorios.
En CMUC, apostamos por la incorporación de técnicas basadas en evidencia, seguras y adaptadas al paciente, que permitan avanzar hacia una cicatrización más rápida y eficaz.
👉 Si te perdiste la primera parte de esta serie, puedes leerla aquí para conocer cómo funciona la técnica HT-MG paso a paso.
Y no olvides seguirnos para descubrir más sobre las nuevas terapias avanzadas en el tratamiento de heridas crónicas.

La radiodermitis, un efecto secundario de la radioterapia: qué es y cómo paliarlo

¿Por qué hay quien no tolera las medias de compresión?
Insuficiencia Venosa Crónica
Tendencia
-

 Divulgaciónhace 7 años
Divulgaciónhace 7 añosLa radiodermitis, un efecto secundario de la radioterapia: qué es y cómo paliarlo
-
 Divulgaciónhace 5 años
Divulgaciónhace 5 años¿Por qué hay quien no tolera las medias de compresión?
-
 Divulgaciónhace 3 años
Divulgaciónhace 3 añosInsuficiencia Venosa Crónica
-

 Productoshace 5 años
Productoshace 5 añosApositos DACC Cutimed Sorbact
-

 Divulgaciónhace 5 años
Divulgaciónhace 5 añosLesiones por humedad
-

 Divulgaciónhace 7 años
Divulgaciónhace 7 añosPresentación de un caso de quemadura por cáusticos en Paciente Diabético
-

 Caso Clínicohace 4 años
Caso Clínicohace 4 añosDermatitis de estasis: a propósito de un caso
-

 Divulgaciónhace 4 años
Divulgaciónhace 4 añosCuras Húmedas y Secas – Diferencias y Usos
































You must be logged in to post a comment Login